CARACTERIZACIÓN FÍSICO-QUÍMICA DE LA CÁSCARA DE PIÑA (ANANAS COMOSUS) TIPO PEROLERA DEL DEPARTAMENTO DE SANTANDER
Walter Pardavé Livia1; Paula Andrea Mendoza Rojas2
1 Magister en Ingeniería, Profesor Titular, Grupo Ambiental de Investigación Aplicada GAIA, Programa de Ingeniería Ambiental, Universidad de Santander UDES, wal.pardave@mail.udes.edu.co.
2 Ingeniera Ambiental, Joven investigador, Minciencias, paulamero10@hotmail.com.
RESUMEN
El desaprovechamiento y la inadecuada gestión de los residuos orgánicos genera una problemática ambiental en las ciudades; esta investigación propone la reutilización de residuos como la cascara de la piña para crear nuevos materiales eco amigables. Con la finalidad de determinar si es viable o no, se hace necesario realizar la caracterización fisicoquímica de la cascara, describiendo detalladamente la realización del proceso, midiendo turbiedad, color, acidez por titulación, punto de ebullición, humedad, solidos suspendidos totales, grados Brix, tamizaje por mallas, análisis del hongo degradante de la cascara a la intemperie y pH. La conclusión principal es que el jugo de la cáscara de piña contiene propiedades favorables para realizar nuevos materiales eco amigables.
Palabras claves: Piña; Cáscara; Caracterización; Biodegradable.

Recibido: 12 de abril de 2023.Aceptado: 19 de Junio de 2023
Received: April 12, 2023.Accepted: June 19, 2023
PHYSICOCHEMICAL CHARACTERIZATION OF PINEAPPLE (ANANAS COMOSUS) PEEL (PEROLERA TYPE) FROM SANTANDER DEPARTMENT
ABSTRACT
The waste and inadequate management of organic waste generates environmental problems in cities; this research proposes the reuse of waste such as pineapple peel to create new eco-friendly materials. In order to determine whether it is feasible or not, it is necessary to perform the physicochemical characterization of the peel, describing in detail the performance of the process, measuring turbidity, color, acidity by titration, boiling point, humidity, total suspended solids, Brix grades, mesh screening, analysis of the degrading fungus from the peel to the weather and PH. The main conclusion is that pineapple peel juice contains favorable properties for making new eco-friendly materials.
Keywrods: Pineapple peel; Characterization, Biodegradable.
Cómo citar este artículo: W. Pardavé, P. Mendoza. “Caracterización físico-química de la cáscara de piña (ananas comosus) tipo perolera del departamento de Santander”, Revista Politécnica, vol.19, no.39 pp.143-159, 2023. DOI:10.33571/rpolitec.v19n38a9
1. INTRODUCCIÓN
La Ananás Comosus más conocida como piña, “pertenece a la familia Bromeliácea, del género Ananás”. Es endémica de América, especialmente del Sur, el primer país en masificarla y exportarla fue Costa Rica. Su forma es cilíndrica y gruesa, con un aproximado de 30 cm de largo y 15 cm de diámetro [1].
La cáscara de la piña actualmente es considera un residuo sólido, el cual, al tener una inadecuada gestión de disposición final, representa focos de contaminación en diferentes entornos de la comunidad, ya que en su proceso de degradación genera hongos, emisión de gases, proliferación de vectores y malos olores.
La caracterización de la cáscara de la piña describe sus propiedades cómo alto contenido en fibra, magnesio y bromelina, enzima que ayuda en la digestión y a reducir la inflamación mediante la eliminación de toxinas en el cuerpo, funcionando, así como un diurético natural. Debido a estas propiedades, se toma agua de cáscara de piña en ayunas ayudando al estómago en absorber mejor los nutrientes y con ello, reducir el riesgo de contraer problemas como artritis, sinusitis, hinchazón abdominal o molestias en la garganta [2].
Lo cual quiere decir que después de extraer los componentes nutricionales de la cascara, ésta se desecha a los residuos no aprovechables llegando finalmente al relleno sanitario.
Los residuos generados por la piña además de la cáscara son: El corazón, la corona y las hojas de la cosecha. De estos residuos se encuentran innovaciones cómo; elaboración de artesanías, alimento para rumiantes, fabricación de papel, fabricación de cuero, hilo, entre otros. De la cáscara de la piña aún no hay ningún uso diferente a las infusiones con fines digestivos.
En la tabla 1 se evidencia los datos de la producción existente en Colombia de aproximadamente 32.700 hectáreas sembradas de piña con las variedades Perolera, MD2 (Oro Miel), Manzana, Cayena lisa [3].
Tabla 1. Área de producción y rendimiento de piña en Santander

Fuente: Evaluaciones Agropecuarias – EVAS [3]
En Santander se están produciendo aproximadamente 506.040 toneladas de piña al año, si el 34.05% de la fruta es cáscara, equivalen a 172.306 Toneladas [4].
Entre los componentes principales de la cáscara están la Hemicelulosa que es un polisacárido no celulósico, que permite la fermentación [5] y los Materiales lignocelulósicos que se encuentran en la biomasa vegetal, estos permiten la obtención de productos sustentables y no contaminantes [5], la disponibilidad de la piña según la época de cosecha se puede observar en la tabla 2.
Tabla 1. Número de usuarios por acueducto

Fuente: https://www.exportropic.com/es/frutas-tropicales/la-pina/
El objetivo de realizar la caracterización fisicoquímica de la cascara de la piña y del jugo que se extrae de ella, es poder analizar si contiene propiedades que permitan usarla cómo materia prima para realizar mezclas en la elaboración de nuevos productos [5].
Se midió la turbiedad del jugo, humedad de sedimentos y de la cáscara seca, solidos suspendidos totales del jugo, color, grados Brix, tamizaje por mallas de la cáscara triturada, acidez por titulación del jugo, análisis de hongo que degrada la cascara a la intemperie, pH del jugo y del mosco que la ayuda a degradar. Con el fin de analizarlos y encontrar un uso físico o propiedades que le permitan ser alternativa a productos existentes que estén generando problemática ambiental en la actualidad.
De la información existente, respecto a los usos de la cascara de la piña se encuentran: - “Evaluación de la capacidad antioxidante de extractos de la cáscara de piña (Ananás comosus), frente a un producto comercial”, - “Subproductos de Piña (Ananás Comosus) como alternativa de alimentación en rumiantes”, - “Uso de harina de maíz y residuos de cáscara de piña como vehiculizantes de especias en la elaboración de un sazonador”, - “Incorporación de harina de cáscara de piña como fuente de fibra en la elaboración de un producto cárnico tipo hamburguesa”, - “Cáscara de Piña como Adsorbente de Colorantes Típicos de la Industria Textil”, entre otros.
2. MATERIALES Y MÉTODO
La caracterización físico-química de la cáscara de la piña se realizó en la Universidad de Santander sede Bucaramanga, en el laboratorio GAIA, dónde se encuentran los equipos necesarios y calibrados para realizar las tomas. El trabajo se desarrolló bajo la metodología design thinking, centrándose en la recopilación de información confiable que permita crear una aproximación al desarrollo y materiales para ejecutar la caracterización.
Para las mediciones se utilizaron equipos cómo mufla, agitador magnético, estufa, trituradora de alimentos, nevera, colorímetro, sonda multiparamétrica, microscopio, entre otros. Elementos cómo probetas, vaso de precipitado, varilla agitadora, celdas, termómetro, pera, pipetas, micro pipetas, vidrio reloj, coladores, recipientes plásticos, aceite de inmersión, asas metálicas, mecheros. e insumos cómo la cascara de piña, el jugo extraído de la cáscara de la piña, reactivos químicos y elementos de protección personal.
2.1 Metodología empleada
El Design Thinking es una metodología de trabajo, que permite crear ideas las cuales se utilizan para solucionar problemas por medio de la innovación convirtiéndolos en proyectos, productos, servicios o áreas. Con el fin de poder ser empleado y útil cómo estrategia para nuevos diseños. Debe ser claro para quien lo lea y si se desea, pueda ser replicada la metodología.
En ésta metodología se describen 4 etapas realizadas:
- a) Definir: La problemática, revisión teórica de soluciones ya existentes con el residuo, fuentes confiables.
- b) Idear: Pruebas y análisis fisicoquímicos necesarios para determinar la caracterización.
- c) Prototipar: Solicitud de los equipos, elementos, reactivos y químicos necesarios para la ejecución de los análisis. Diseño de los montajes para realizar las pruebas de caracterización. Extracción del jugo de la cascara.
- d) Probar: Realizar los montajes y posteriormente las pruebas de caracterización, utilizando el jugo extraído. Y de la cáscara triturada y seca. Analizar los resultados teniendo en cuenta los cambios del jugo al estar expuesto al ambiente ya que al ser orgánico presenta cambios bruscos en tiempo corto; como fermentación y generación de hongos.
En las Figuras 1 y 2 se describe la metodología implementada para el desarrollo de este trabajo investigativo.
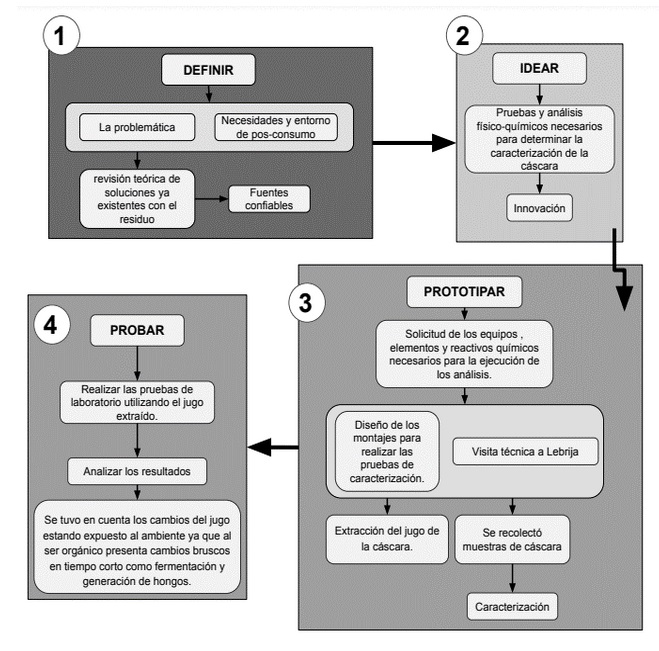
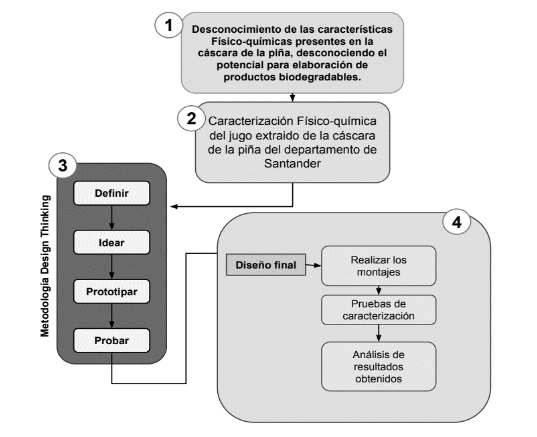
Figura 2. Metodología de trabajo implementada
2.2 Recolección de muestra
Se recolectó la muestra de los residuos de la cáscara de piña, en un establecimiento comercial ubicado en el municipio de Bucaramanga, hace parte de la variedad de piña denominada Perolera, se peló en el establecimiento y se transportó hasta el laboratorio en bolsa plástica. Se realizó la caracterización al día siguiente.
2.2.1 Preparación de la Cáscara de Piña
En las Figuras 3 y 4 se observa el proceso de cómo se recibió la muestra, su selección identificando la más sana, luego se retiró el exceso de fruta adherida a la cascara por medio de una cucharilla metálica, quedando lista para la caracterización.
s=

Figura 3. Selección de la cáscara más sana y pareja

Figura 4. Cáscara seleccionada para caracterización
Fuente: Autores
Con la cáscara libre de fruta, se procedió a triturarla y tomar las diferentes muestras que fueron, exprimirla almacenando ese jugo, recoger la cáscara exprimida y dejarla secar., del jugo que se extrajo, se dejó reposar y se observo formación de sedimento el cual también fue muestra de estudio.
3.RESULTADOS
En las Figuras 5, 6 y 7 se puede observar el proceso de extracción del sedimento utilizado para el muestreo. La extracción se realizó por medio de una micropipeta, se añadió una pera y se extrajo el sedimento de las muestras; almacenando el contenido en vasos de precipitado de vidrio.
En la caracterización fisicoquímica se realizaron mediciones de: turbiedad, color, acidez por titulación, punto de ebullición, humedad, solidos suspendidos totales, grados Brix, tamizaje por mallas, análisis del hongo que degrada la cascara a la intemperie, pH, obteniendo los siguientes resultados:
Muestra n1 = Sedimento 1: se exprimió el 11 noviembre de 2022 Refrigerada a -4ºC en vaso de precipitado de vidrio envuelto con papel vinipel para evitar contaminación. hasta la fecha de toma de muestras (23 Nov) 12 días de refrigeración. Sin cambio aparente de color ni olor.
Muestra n2 = Sedimento 2: se exprimió el 21 noviembre de 2022 Refrigerada a -4ºC en vaso de precipitado de vidrio envuelto con papel vinipel para evitar contaminación de la nevera, hasta la fecha de toma de muestras (23 Nov) 2 días de refrigeración.

Figura 5. Muestra 1 completa 12 días de refrigeración

Figura 6. Muestra 2 completa 2 días de refrigeración

Figura 7. Sedimento de la muestra 1 y sedimento de la muestra 2
Fuente: Autores
La toma de los parámetros se llevó a cabo el 23 de Nov de 2022 en horas de la tarde.
3.1. Turbiedad:
En la Figura 8 se observa el colorímetro marca Hach utilizado para realizar la medición.

Figura 8. Colorímetro programado para medir turbiedad
Fuente: Autores
3.1.1 Turbiedad:
Muestra n1: Con dilución de 1ml de muestra en 99ml de agua destilada para un total de 100ml. Resultado = 113 FAU
Muestra n2: Con dilución de 1ml de muestra n2 en 99ml de agua destilada para un total de 100ml. Resultado = 149 FAU
3.1.2 En liquido:
Muestra n1: Con dilución de 1ml de Liquido en 99ml de agua destilada para un total de 100ml. Resultado = 44 FAU
Muestra n2: Sin dilución Resultado: 305 FAU
3.1.3 En mezcla de sólido y liquido: Con dilución de 1ml de Liquido en 9ml de agua destilada para un total de 10ml. Resultado = 525 FAU
Para realizar el análisis de turbiedad de las muestras fue necesario realizar diluciones ya que el jugo se encontraba en una concentración muy alta, pasando el rango de lectura del colorímetro, por lo tanto, se realizaron iniciando con 10ml si seguía siendo +++, se pasaba a 100ml. Los resultados se muestran en la tabla 3.
Tabla 3. Resultados de medición de Turbiedad

Fuente: Autores
3.2. Sólidos en suspensión:
3.2.1 En sedimento:
Muestra n1: Con dilución de 1ml de muestra en 99ml de agua destilada para un total de 100ml. Resultado = 106 TSS mg/L
Muestra n2: Con dilución de 1ml de muestra n2 en 99ml de agua destilada para un total de 100ml. Resultado = 134 TSS mg/L
3.2.2 En liquido:
Muestra n1: Con dilución de 1ml de Liquido en 99ml de agua destilada para un total de 100ml. Resultado = 38 TSS mg/L
Muestra n2: Sin dilución Resultado = 241 TSS mg/L
3.2.3 En mezcla de sólido y liquido:
Con dilución de 1ml de Liquido en 9ml de agua destilada para un total de 10ml. Resultado = 541 TSS mg/L
Para realizar el análisis de sólidos en suspensión de las muestras fue necesario realizar diluciones ya que el jugo se encontraba en una concentración muy alta que pasa el rango de lectura del colorímetro, por lo tanto, se realizaron iniciando con 10ml si seguía siendo +++, se pasaba a 100ml.
El sedimento que se formó en el fondo mostraba una apariencia arenosa, y se evidencia en los resultados con la alta concentración de estos. En la tabla 4 se muestran los resultados obtenidos.
Tabla 4. Resultados de medición de SST

Fuente: Autores

Figura 9. Sonda multiparamétrica marca Hanna programada en lectura de pH.

Figura 10. Sonda multiparamétrica Realizando lectura de la muestra
Fuente: Autores
En sedimento:
Muestra n1 =4.87
Muestra n2 =6.30
En liquido:
Muestra n1 =6.71
Muestra n2 =6.6
Mezcla de sólido y liquido=4.24
Según la escala de pH el jugo en general se encuentra en un rango acido con 4.24, y el jugo sin el sedimento se acerca a neutro con un pH de 6.71. El sedimento podría estar acidificando el jugo en general, ayudando en procesos de degradación, fermentación, acelerando o deteniendo la proliferación de hongos.
Tabla 5. Resultados de medición de pH

Fuente: Autores
3.4 Grados Brix
En la Figura 11 se observa el instrumento utilizado para la medición sin muestra y en la Figura 12 se observa el resultado obtenido. Se midió en una escala de 0 – 90% permitiendo conocer la cantidad de sacarosa que posee la cáscara de la piña.

Figura 11. Refractómetro sin muestra

Figura 12. Refractómetro con muestra
Fuente: Autores
Sedimento del jugo = 2%
Jugo de la cáscara con sedimento (exprimido 1dic) medido (2dic) = 3%
Liquido sin sedimento = 2.5%
En la tabla 6 se pueden observar los resultados obtenidos en la medición del porcentaje de sacarosa. El resultado revelado por el refractómetro en el jugo extraído de la cáscara de la piña es muy bajo ya que en una escala de 0% a 90% fue menor al 3%.
Tabla 6. Resultados de medición de Grados Brix

Fuente: Autores
3.5 Color
En sedimento:
Muestra n1: Con dilución de 1ml de muestra en 999ml de agua destilada para un total de 1000ml. Resultado = 77 Pt Co
Muestra n2: Con dilución de 1ml de muestra n2 en 999ml de agua destilada para un total de 1000ml. Resultado = 64 Pt Co
En liquido:
Muestra n1: Con dilución de 1ml de Liquido en 99ml de agua destilada para un total de 100ml. Resultado = 189 Pt Co
Muestra n2: Con dilución de 1ml de Liquido en 99ml de agua destilada para un total de 100ml Resultado = 70 pt Co
En mezcla de sólido y liquido: N/A
Para realizar el análisis de color de las muestras fue necesario realizar diluciones ya que el jugo se encontraba en una concentración muy alta pasando el rango de lectura del colorímetro, por lo tanto, se realizaron iniciando con 10ml de agua destilada, si seguía siendo +++, se pasaba a 100ml, si seguía siendo indetectable se diluía en 1000ml. Al final el resultado se multiplicó por la dilución realizada. En la tabla 7 se pueden observar los resultados obtenidos.
Tabla 7. Resultados de medición de Color

Fuente: Autores
3.6 Acidez por titulación
En las Figuras 13, 14 y 15 se observa el procedimiento para realizar el proceso de la titulación, primero se agregó el sobre de fenolftaleína a la muestra, se agregó el NaOH por goteo y cuando se mostró el cambio de color en la muestra, se pudo conocer la cantidad en ml de NaOH necesaria para determinar la acidez, el cálculo se realizó mediante la siguiente formula.
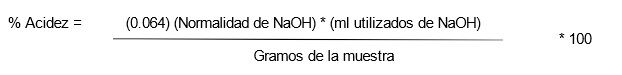

Figura 13. Sobre de fenolftaleína agregado para indicar la titulación

Figura 14. Bureta con NaOH

Figura 15. Cantidad de NaOH utilizado para notar cambio de color
Fuente: Autores
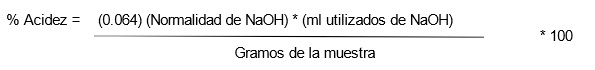

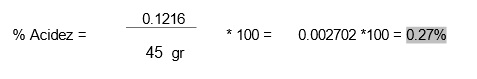
3.7 Punto de ebullición
En las Figuras 16, 17 y 18 se observa parte del procedimiento para realizar la medición, en el cual se puso a hervir la muestra en un vaso de precipitado, sobre una estufa con placa de calentamiento, llevando el control de la temperatura por medio de un termómetro.

Figura 16. jugo extraído de la cáscara llegando a punto de ebullición

Figura 17. temperatura del punto de ebullición

Figura 18. pasado el punto de ebullición forma un melado con olor dulce
Fuente: Autores
- * 85°C – 90°C
Cuando el jugo extraído de la cáscara de la piña llega al punto de ebullición, se vuelve viscoso, empieza a formar grandes burbujas y se torna en un color amarillo quemado, empezando a formar en el fondo del recipiente un sedimento color café y desprende un olor dulce.
3.8 Humedad
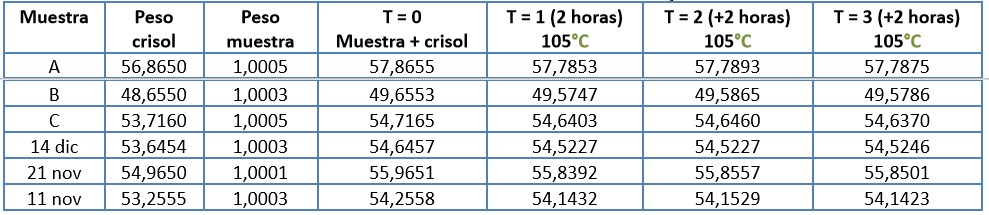
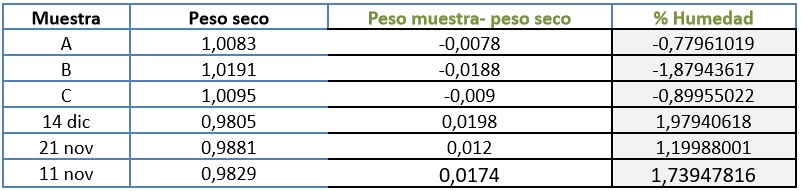
Para realizar la medición, se pesó el crisol previamente seco en horno, se taró la balanza analítica y se pesó la muestra inicial luego se introdujo el crisol con la muestra en el horno a 105ºC, a las 2 horas se retiró del horno se pasó por desecador y se pesó nuevamente, se registraron los datos y se repitió el proceso 2 veces más, los resultados se pueden observar en la tabla 8.
Sedimento
Muestra n1 sedimento 1: 3.278%
Muestra n2 sedimento 2: 2.495%
Cáscara triturada y seca tamizada bajo malla #40:
Tabla 8. Resultados de medición de Humedad bajo malla #40
Fuente: Autores
3.9 Tamizaje por mallas
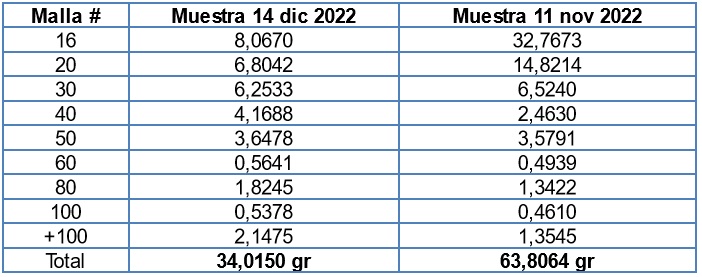
En la tabla 9 se registraron los resultados del proceso de tamizaje de la cáscara triturada, exprimida, seca a la intemperie y finalmente molida.
Peso en (gr) tamizados:
Muestra 14 dic 2022: 34,1929 gr
Muestra 11 nov 2022: 64,4075 gr
Tabla 9. Resultados de tamizaje de la Cáscara triturada, exprimida, seca a la intemperie y finalmente molida
Fuente: Autores
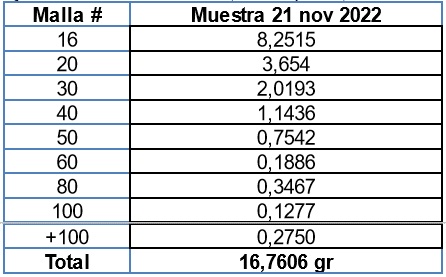
En la tabla 10 se registraron los resultados del proceso de tamizaje de la cáscara triturada, sin exprimir, seca a la intemperie y finalmente molida.
Peso en (gr) tamizados:
Muestra 21 nov 2022: 16,7698 gr
Tabla 10. Resultados de tamizaje de la cáscara triturada, sin exprimir, seca a la intemperie y finalmente molida
Fuente: Autores
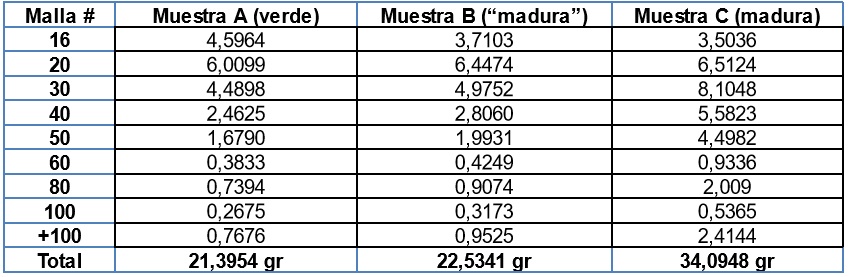
En la tabla 11 se registraron los resultados del proceso de tamizaje de Cáscara triturada, sin exprimir, seca en horno por 20 horas a 105°C y finalmente molida.
Peso en (gr) tamizados:
Muestra A (verde): 21,3954 gr
Muestra B (“madura”): 22,5341 gr
Muestra C (madura): 34,1032 gr
Tabla 11. Resultados de tamizaje de la cáscara triturada, sin exprimir, seca en horno por 20 horas a 105°C y finalmente molida
Fuente: Autores
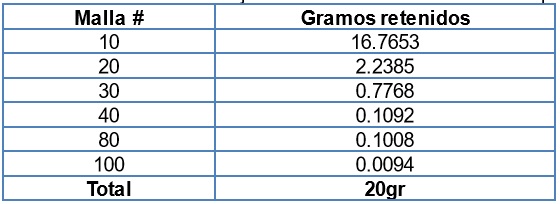
En la tabla 12 se registraron los resultados del proceso de tamizaje de 20gr de cáscara triturada seca sin exprimir.
Tabla 12. Resultados de tamizaje de cáscara triturada seca sin exprimir
Fuente: Autores
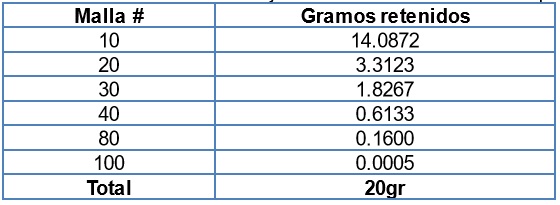
En la tabla 13 se registraron los resultados del proceso de tamizaje de 20gr de cáscara triturada seca exprimida.
Tabla 13. Resultados de tamizaje de cáscara triturada seca exprimida
Fuente: Autores
3.10 Hongo descomponedor de la cáscara
En las Figuras 19, 20 y 21 se puede observar el proceso de tinción e identificación del hongo que descompone naturalmente la cáscara.

Figura 19. Hongo degradante de la cáscara de piña

Figura 20. Tinción del hongo con azul de metileno

Figura 21. Montaje de los hongos, productos de la degradación de las cáscaras
Fuente: Autores
3.11 RESULTADOS
Se dejó el jugo a la intemperie en tres modos, dos en vaso de precipitado de vidrio, uno cubierto con vinipel y el otro con papel aluminio, y el tercero en frasco de vidrio, con tapa de rosca. Los dos primeros vasos, mostraron los cambios iniciales y presentaron presencia de hongos. Y el tercero solo presencia de sedimento y un poco de alteración en el color, oscureciéndose.
El jugo extraído de la cáscara se mostró muy sensible a la temperatura ambiente, ya que empieza a presentar cambios en su coloración, tornándose más oscura, forma un sedimento blanco, el olor es fuerte y desprende gases. Produce fermentación. Después de permanecer a la intemperie por un par de días presenta presencia de hongos.
El hongo presente en los vasos inicialmente tenía un aspecto de coliflor, blanco con formas onduladas, al pasar de los días fue cambiando, presentando pudrimiento y al final una nata espesa flotante, de color oscuro, con olor muy fuerte y poco agradable.
El hongo que se genera en el lixiviado de la cáscara, es de color piel y gelatinoso estando en contacto con el líquido, pero al retirarlo del líquido del lixiviado, se empieza a secar y se torna de color café oscuro, al pasar de 11 días se puede observar que toma semejanza a la estructura del papel kraft. Al analizarlo en microscopio se observan fibras vegetales entrelazadas.
4. DISCUSIÓN
Tener en cuenta el tiempo de degradación de la cáscara, se “pudre” muy fácil y dura más de 20 días en secarse completamente estando expuesta a la intemperie. Al dejar la cáscara degradando a la intemperie extendida, sin exprimirse ni triturarse, empieza a desprender olores muy fuertes, los dos o tres primeros días son agradables, de fermentación cómo guarapo, pero si se almacena en bolsa a partir de los cinco días es un olor desagradable de descomposición, a partir de los 15 días es un olor fétido muy fuerte difícil de eliminar del ambiente. Suelta bastante lixiviado, manchando la superficie en la que se encuentre y el cual al irse secando se va volviendo pegajoso, se presenta la formación de un hongo a partir del lixiviado, de color blanco con tonos piel, de textura gelatinosa y compacto (se deja levantar sin destrozarse).
Cuando el jugo es recién exprimido, se envasa en un frasco de vidrio con tapa de rosca y se lleva a refrigeración con una temperatura de -4°C en la cual se mantiene y no presenta alteraciones. Cuando la muestra se retira de refrigeración y tiene contacto con el ambiente, empieza a generar reacción, por lo tanto, se recomienda utilizarla inmediatamente.
Al momento de maduración en el cultivo se agrega una gota de etrel en el centro de la flor de la piña logrando un color amarillo que permite venderla mejor. Pero al momento de analizar la cáscara que aún no estaba y la recolectaron verde, muestra presencia de un hongo verde, mientras que en la cáscara que estaba realmente madura no presenta ningún tipo de hongo al secarla a la intemperie.
La cáscara de la piña seca a la intemperie, tiene un olor característico a abono ya que paso por un proceso completo de degradación con formación de hongos, emisión de gases y demás, mientras que la cáscara que se secó en horno por 20 horas tiene un olor dulce y bastante agradable. Ya que no sufrió dicho proceso y que el calor incrementa sus propiedades entre esas el olor.
5. CONCLUSIONES
La caracterización realizada a la cáscara de la piña nos permite ampliar la información bibliográfica existente en la web, ya que en relación al tema de caracterización fisicoquímica no se encuentra mayor información.
La cáscara de la piña muestra aspectos positivos ya que contiene propiedades que le facilitan y permiten la unión entre moléculas creando uniones los cuales a gran escala generan el subproducto de base biológica, el cual aún está en proceso de investigación y desarrollo.
6. REFERENCIAS BIBLIOGRÁFICAS
Articulos:
[1] Yendry R. Corrales-Ureña, CarlosVillalobos-Bermúdez, Reinaldo Pereira, MelissaCamacho, Eugenia Estrada, OrlandoArgüello-Miranda & Jose R.Vega-Baudrit. (2018). Biogenic silica-based microparticles obtained as a sub-product of the nanocellulose extraction process from pineapple peels. Scientific reports (2018) 8:10417. Pág. 1-9.
[2] Ti Li, Peiyi Shen, Wei Liu, Chengmei Liu, Ruihong Liang, Na Yan y Jun Chen. (2014). Principales polifenólicos en cáscara de piña y sus interacciones antioxidantes. Revista internacional de propiedades alimentarias, 17. Pág. 1805–1817
[3] Nathalie Gontard, Ulf Sonesson, Morten Birkved, Mauro Majone, David Bolzonella, Annamaria Celli, Hélène Angellier-Coussy, Guang-Way Jang, Anne Verniquet, Jan Broeze, Burkhard Schaer, Ana Paula Batista & András Sebok (2018). A research challenge vision regarding management of agricultural waste in a circular bio-based economy. Critical reviews in environmental science and technology 2018, Vol. 48, No. 6. Pág. 614 – 654.
[4] Swabiiha Buxoo Pratima Jeetah (2020). Feasibility of producing biodegradable disposable paper cup from pineapple peels, orange peels and Mauritian hemp leaves with beeswax coating. SN Applied Sciences (2020) 2:1359. Pág. 1 – 15.
[5] Nurul Ain Ab Jalil, Nur Asyikin Mokhtaruddin, Chin Hua Chia , Irfana Kabir Ahmad, Mohamad Jani Saad, and Mahanim Sarif. (2022). Physical and Chemical Characteristics of Agricultural-Plastic Wastes for Feasibility of Solid Fuel Briquette Production. Sustainability 2022, 14, 15751. Pág. 1-13
[6] Gaofeng Yuan, Hua Lv, Bingjie Yang, Xiaoe Chen, and Haiyan Sun (2015). Physical Properties, Antioxidant and Antimicrobial Activity of Chitosan Films Containing Carvacrol and Pomegranate Peel Extract. Molecules 2015, 20. Pág. 11034-11045
[7] Pranav D. Pathak, Sachin A. Mandavgane, and Bhaskar D. Kulkarni. (2017). Fruit peel waste: characterization and its potential uses. Current Science, Vol. 113, No. 3. Pág. 1 – 11.
[8] Nathalie Gontard, Ulf Sonesson, Morten Birkved, Mauro Majone, David Bolzonella, Annamaria Celli, Hélène Angellier-Coussy, Guang-Way Jang, Anne Verniquet, Jan Broeze, Burkhard Schaer, Ana Paula Batista & András Sebok (2018). A research challenge vision regarding management of agricultural waste in a circular bio-based economy. Critical reviews in environmental science and technology 2018, Vol. 48, No. 6. Pág. – 654.
[9] Swabiiha Buxoo Pratima Jeetah (2020). Feasibility of producing biodegradable disposable paper cup from pineapple peels, orange peels and Mauritian hemp leaves with beeswax coating. SN Applied Sciences (2020) 2:1359. Pág. 1 – 15.
[10] Jyoti Jatav, Ayon Tarafdar, Chakkaravarthi Saravanan , and Bhaswati Bhattacharya (2022). Assessment of Antioxidant and Antimicrobial Property of Polyphenol-Rich Chitosan-Pineapple Peel Film. Journal of Food Quality. Pág. 1 – 10.